电解液是一种可以导电的溶液,分别由溶剂和溶质组成。溶剂化是指溶剂分子围绕溶质离子形成的溶液结构,这种结构在电解液中发挥着重要的作用。以下是用氧键解释电解液中溶剂化结构的相关内容:
电解液作为电池中四大材料之一,与正极、负极均有相互作用,电池中的有益的、无益的反应均发生在电解质和电极的界面,界面反应与溶剂-溶质相互作用密切相关。
近来读了一篇中科院金属所李峰老师的文章《为低温锂金属电池设计温度不敏感的溶剂化电解质》“Designing Temperature-Insensitive Solvated Electrolytes for Low-Temperature Lithium Metal Batteries”,里面提出”配位氧键“的说法,简单来说,EC、PC、SL这些高介电常数溶剂是氧供体溶剂,氧的强电负性完全阻止了Li+和阴离子的配位,使得电解液中Li+以溶剂分离离子对(SSIP)的形式存在,Li+与溶剂直接配位,阴离子不能直接与Li+配位。这种情况导致的结果是,由于氧供体溶剂的强电负性,限制了(锂金属电池)在低温下的可逆性和动力学性能。其它文献[2]也认为:电解质溶剂化壳层(solvation sheath)的脱溶剂化过程是在超低温下工作的锂离子电池的控制步骤。
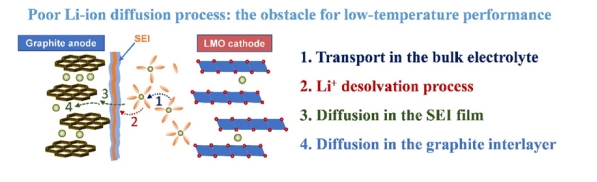
在低温下工作的典型锂离子电池配置中锂离子扩散途径的关键步骤
溶剂分离离子对(SSIP,solvent-separated ion pair):Li+与一些溶剂强配位,Li+淹没在溶剂的汪洋大海中,难以脱身;弱溶剂化电解液的理念来源于此。
紧密接触离子对(CIP,contact-ion pair):一个Li+与一个阴离子配位。Li+在溶剂的汪洋大海中终于找到一叶扁舟。一个Li+与一个阴离子配位,共同参与SEI的形成,SEI富含LiF、LiPO4
小聚体(AGG,aggregation):多个Li+与一个阴离子配位。例如高浓度电解液。
纳米簇(cluster):由CIP、AGG组成的一个群体。
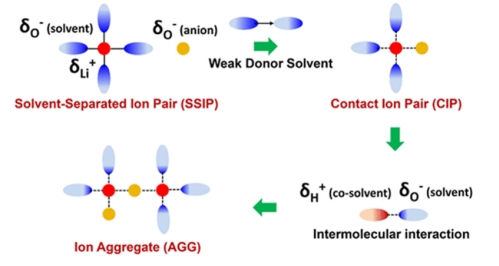
图 1.电解质的设计原理:通过调节供体溶剂的电负性实现溶剂化设计的示意图。
Figure 1. Design principles and solvation regulation of the electrolyte: schematic illustration of the solvation design by electronegativity regulation of the donor solvents.
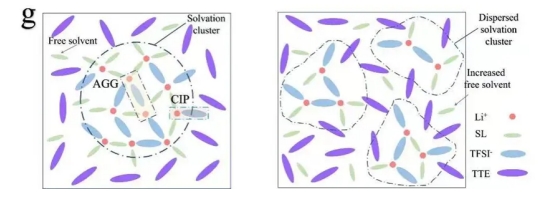
局部高浓度电解液中溶剂化团簇结构示意图[3]
Figure 2. Schematic structure of solvation clusters in the localized high-concentration electrolyte.
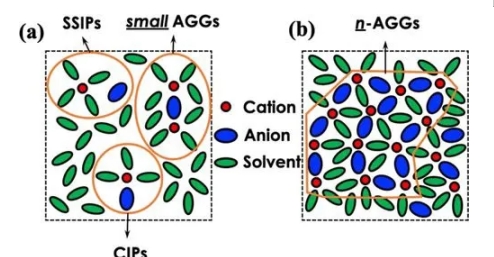
图 溶剂化结构示意图(a)SSIP、CIP和AGG;(b)纳米簇
解决办法:用一种非溶剂共溶剂来减弱醚类溶剂中供体氧的电负性,使阴离子供体参与到Li+的溶剂化结构中。具体来说,用TTE这种不溶解锂盐的溶剂作为共溶剂,加入THF等醚类混合溶剂中,来调整溶剂化结构。文章认为DMC、DOL、DME、THF、2MeTHF(2-methyltetrahydrofuran)等都是弱供体溶剂,有氧,但是电负性较弱,允许Li+和阴离子结合,在低浓度电解质中形成CIP和AGG。THF和2MeTHF被选为具有较弱电负性和最佳还原稳定性的溶剂,用TTE这种不能与Li+配位的供体溶剂,进一步减弱MixTHF(THF+2MeTHF)的电负性,在LFP/Li电池中获得优良的低温与电化学循环性能。文中通过观察峰位的移动来判断各组分之间的相互影响,值得学习。文章应用醚类电解液,虽然DME、THF等溶剂对金属锂具有还原稳定性,但是却不耐氧化,在高电压体系中无法应用,所以文中只能采用LFP作为研究对象,LFP的面容量1.5mAh/cm2,很低。用一种低容量正极LFP与一种高容量负极Li进行匹配,NP比6,也许不具备产业化价值,但是这种电解液的设计思路,尤其是从氧的角度来进行解释,继氢键、锂键后又提出了氧键,这一点我个人认为是最大的创新。
本文原标题为用氧键解释电解液中溶剂化结构,有利于行业对镀液进一步的了解,文章转载自网络,版权归原作者所有。
更多表面处理文章,敬请关注公众号:易镀
易镀,是深圳市恒享表面处理技术有限公司旗下专为电镀行业打造的信息服务平台,分享金属行情、产品测评、电镀液配方、电镀视频、电镀问答等,以专业解决各种金属表面处理难题为旨,不断优化电镀解决方案,促进电镀行业的发展。表面处理难题,找易镀,详情请咨询:13600421922(程生)


Copyright © 2021 深圳市恒享表面处理技术有限公司 All Rights Reserved 备案号:粤ICP备09192382号 技术支持:易百讯 - 深圳网站建设